遺伝子の正常な機能を回復し、「がん」の無限増殖を停止する癌遺伝子治療
〒810-0041 福岡市中央区大名2-6-39 7F フリーダイヤル:0120-760-077 /TEL:092-707-1710
診療カレンダー・予約フォーム 診療カレンダー

がん
遺伝子治療
「がん」の発生と成長の根本的な
原因を断つ、
新しいがん治療の選択肢
がん遺伝子治療の特徴
がん遺伝子治療は、本来すべての人の体内に備わっているがん抑制遺伝子の機能を回復させてがんを抑制する治療です。
がん細胞の発生や成長の根本的な原因である「遺伝子の異常」に対してアプローチし、身体が本来持っているがん抑制遺伝子を再び機能させてがんをアポトーシス(自死)に導きます。
副作用が少ない
難治性がんまで適用
放射線治療との併用可能
効果が期待できる
がん抑制遺伝子
細胞のがん化を抑制する仕組みを持った遺伝子
がんの発生と成長を未然に防ぐ働きを持った遺伝子をがん抑制遺伝子といいます。がん抑制遺伝子には細胞が破壊されても、細胞のがん化を防ぐ機能が備わっています。
この機能は、細胞内の遺伝子にプログラムされています。このプログラムが毎日適切に働くことで、私たちの身体の細胞はがん化のリスクから守られており、細胞のがん化にストップをかけています。がん抑制遺伝子の三大機能が下記の3種です。
1.壊れた細胞の機能を修復する
DNAが損傷を受けると、修復酵素が駆けつけて、こうした傷を修復します。
2.細胞を死滅させる(アポートシス)
がんを異物と捉えて殺傷するのではなく、その性質を正常に戻すことにより、がん細胞の「自殺」ないしは「老化」の誘導
3.細胞の増殖を停止する
「がん遺伝子(がんの無限増殖を促すライセンシングファクターを含む)」の異常増殖を停止
がん抑制遺伝子が壊れてしまうと、上記3種の働きを行うことができません。壊れたまま放置された細胞は制御ができなくなり無限に増殖を続け、やがて「がん発症」となります。 そこで、一度失われたがん抑制機能を回復するために、「がん抑制遺伝子」を再びがん細胞へ導入することにより細胞本来の機能を回復して自らの力でがんと闘う治療が「遺伝子療法」です。
がん抑制遺伝子の三大機能の役割と比較
がん抑制遺伝子の損傷とがん発生のメカニズム
健康な方
がん抑制遺伝子が
機能している状態
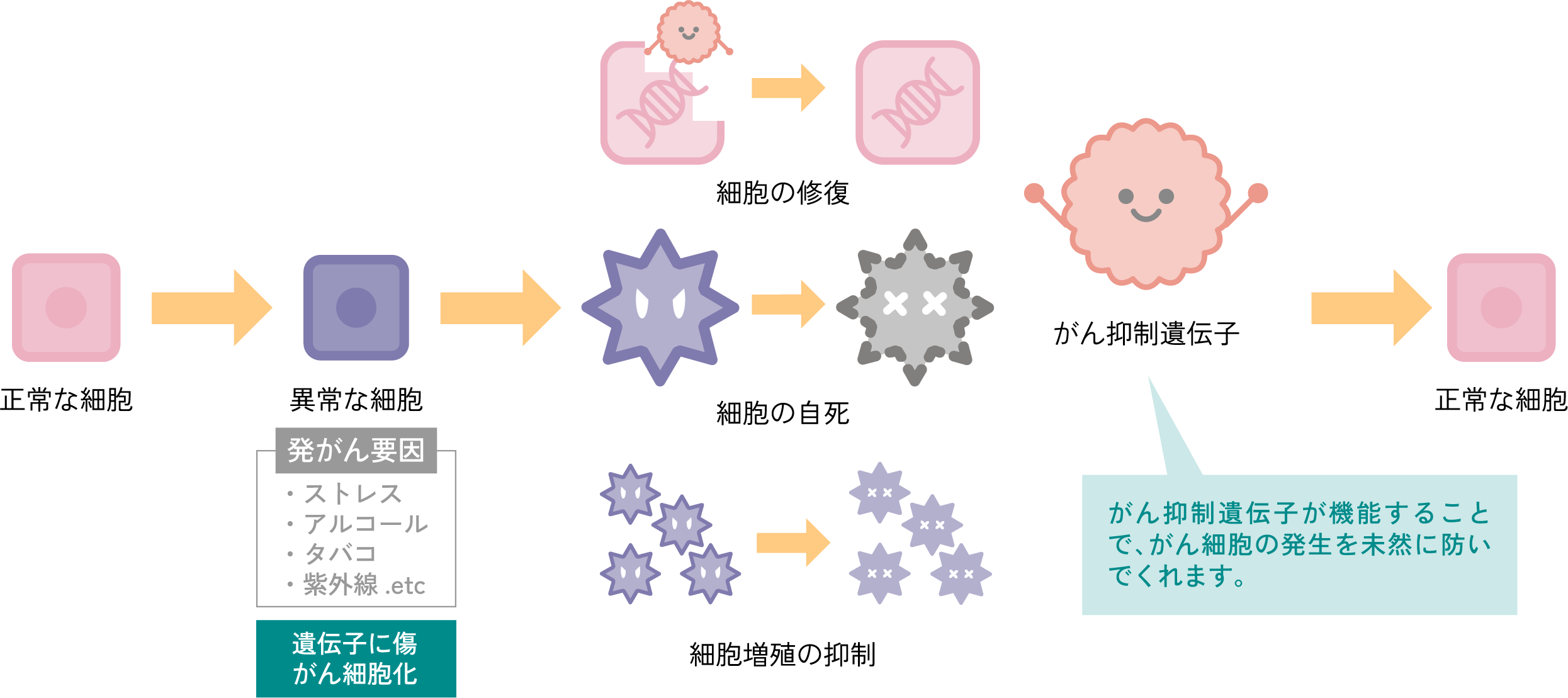
細胞に問題が発生してもがん細胞の発生を未然に防いでくれる。

がんにはならない
がん患者様
がん抑制遺伝子が
機能していない状態
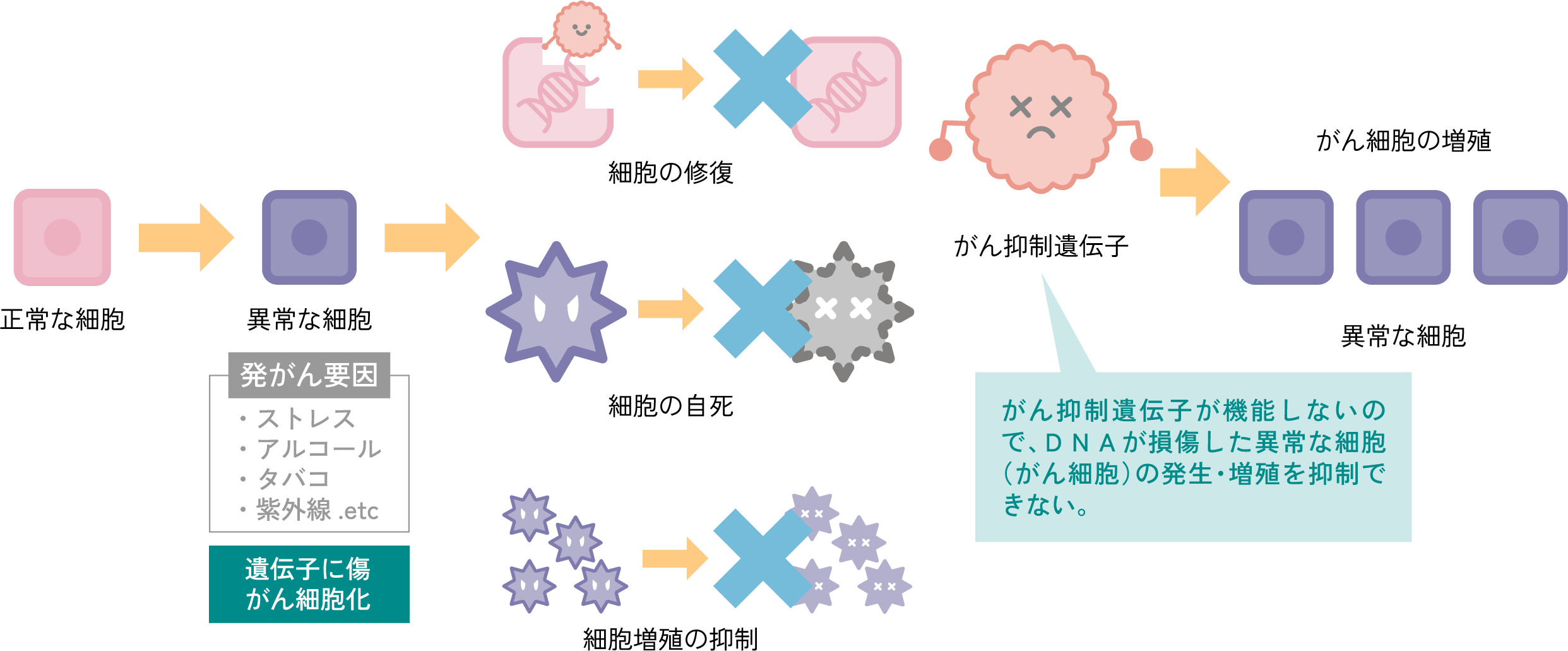
がん抑制遺伝子が壊れてしまうと、機能せずがん細胞の発生と成長を止めることができない。

がんになる
遺伝子治療の方法
遺伝子治療の目的はがん抑制遺伝子の三大機能(修復・自死・抑制)を復活させること
がん抑制遺伝子が壊れたがん患者様に対して点滴でがん細胞にがん抑制遺伝子を導入しがん細胞の核の中にまで入れることで、三大機能を回復し細胞分裂のサイクルを正常化させ、体内から自然にがん細胞が消えていくような環境を作ります。
遺伝子治療
により
がん抑制遺伝子が
機能している状態
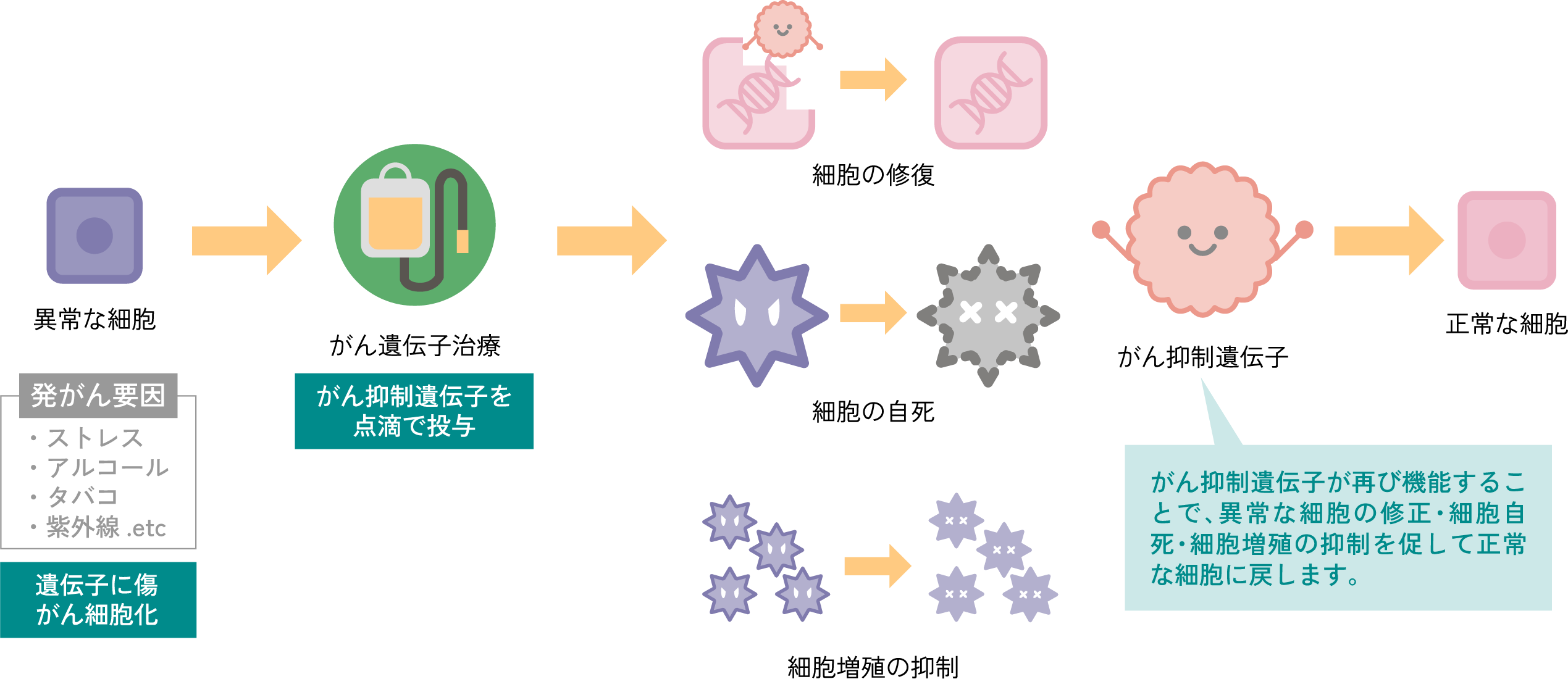
一度失われた、がん抑制機能の回復のため、がん抑制遺伝子を外からがん細胞へ導入する。
からだ本来の機能を回復して、
自らの身体の力でがんと闘う
それが「がん遺伝子治療」です
世界で行われている遺伝子医療
2018年には先進医療国である米国をはじめ欧州、中国、ロシア、全世界で遺伝子治療の研究が行われ複数の国で承認製薬が使用されるまでに至っています。

アメリカ
2015年 悪性黒色腫(メラノーマ)
2017年 網膜ジストロフィ

欧 州
2012年 LPL欠損症
2016年 ADA欠損症
2016年 欧州 高リスク造血器
悪性腫瘍

ロシア
2011年 重症下肢虚血を含む末梢動脈疾患

中 国
2003年 頭頸部扁平上皮癌(HNSCC)
2006年 鼻咽頭癌

フィリピン
2006年 化学療法抵抗性 膵癌、
骨肉腫、軟部
体内に正常な遺伝子を送り込んで病気を治す遺伝子医療は、1990年に米国にて免疫不全症の治療に試みられてから世界的に研究が進んできました。
遺伝子治療技術は格段に進歩し、世界で遺伝子治療薬の実用化が進んでます。中でも「がん」については世界中で研究が進められ、遺伝子治療臨床試験の65%を占めています。
近年では、遺伝子医療技術の安全性の向上により、特定の遺伝性疾患に限られていた治療の領域もあらゆる難治性疾患に広がっています。
従来の治療に加え新しいがん治療の選択肢となることが期待されており、多くの国で承認製剤が発売されるに至っています。
遺伝子治療の特徴
- 副作用が少ない
- がん抑制遺伝子の使用では、正常細胞への悪影響がありません。そのためほとんど副作用がなく、高齢者やがんが進行した方でも対応可能です。
- 抗がん剤や放射線との相乗作用
- 抗がん剤や放射線など他の治療を受けている場合でも影響なく受けることが可能です。抗がん剤に耐性を持っているがん細胞にも有効なため兼用することで相乗効果が得られます。
- 再発・転移にも効果が期待できる
- 点滴により全身に作用するため新しいがんの発生を抑えることが期待できます。
- 通院での治療が可能
- 治療方法が点滴での投与のため麻酔や入院は不要です。日常生活を普段通りに過ごしながら通院で治療可能です。
- 正常細胞に影響を与えない
- がん抑制遺伝子は正常なもともと人の体に備わっているものなので、投与しても正常細胞に影響を与えることはありません。
- 耐性とならない
- がん遺伝子治療に用いるものはがん細胞の核の中で作用するので耐性になることがありません。
- がん幹細胞や難治性のがんにも治療可能
- がん遺伝子治療は遺伝子に直接作用するため、多数のがんに適応可能です。抗がん剤に反応しにくいがん細胞や抗がん剤が耐性になったがん細胞や胸腺腫や中皮腫・肉腫にも期待できます。
- がんの種類を問わない
- がんの原因である遺伝子異常に作用するためがんの種類や部位を問わず有効です。また血管やリンパ管を通り全身の細胞に巡らせるのでがんの適応範囲も広いです。
遺伝子治療で対応できる主な「がん」
適応するがんの種類一覧
頭頸部
- 咽頭がん
胸 部
- 肺がん
- 小細胞肺がん
- 乳がん
肝臓・胆のう・膵臓
- 肝臓がん
- 胆管がん
- 膵臓がん
消化器
- 食道がん
- 胃がん
- 大腸がん
泌尿器
- 腎臓がん
- 膀胱がん
- 前立腺がん
女性特有
- 子宮頸がん
- 子宮体がん
- 卵巣がん
全 身
- メラノーマ
- 原発不明がん
- など

がん遺伝子治療は「がん」の種類や進行度を問わず、他治療と併用できるなど
適応の幅が大変広いのも特徴です。
一人ひとりの「がん」に合わせた
テーラーメイド型での治療提案
「がん」と遺伝子の関わりは、「がん」の種類によって異なることが分かっています。
当院では、14種の遺伝子から患者様一人ひとりの「がん」の種類や状態に合わせてこれらを組み合わせることで、幅広い「がん」に対して適応が可能となっています。
p53
- ●傷ついた遺伝子を修復する働きを持つ。
- ●がん化した細胞を自死(アポトーシス)してくれる役割を持つ
- ●ゲノムの管理人とも呼ばれる
PTEN
- ●がんの新生血管形成を阻害し、がん細胞に栄養が行かないように働く
- ●がんの激しい増殖に最も関与している抑制遺伝子
p16
- ●異常な細胞分裂をストップさせ増殖を防ぐ
- ●p53を阻害するMDM2の働きを抑えp53の働きを活性化させる
SMAD4
- ●異常な細胞分裂を防ぐ
- ●SMAD4に異常が生じるとTGFβの細胞増殖抑制作用が消失し、細胞増殖が促進される
ARID1A
- ●ARID1A遺伝子は、様々な遺伝子あらわれるのを促進するタンパク質を作ります。
- ●卵巣明細胞がん、子宮内膜がん、卵巣類内膜がんなどの女性のがんや、胃がん、胆管がんなどで欠損しています。
RB1
- ●RB1が不活性化すると腫瘍細胞の増殖に有利な環境になる。
- ●さらに、RB1の不活性化により、炎症などに関与するタンパクが増加し、血管新生を促す。
APAF-1
- ●APAF-1は「Apoptosis Protease-activating Factor 1」の略で、がん細胞の自死(アポトーシス)に大きく関わるタンパク質です。
PSMD10(ガンキリン)抑制RNA
- ●ガンキリンは腫瘍を抑制する腫瘍抑制因子を死滅させる働きがあり、抑制遺伝子が本来の機能を果たせず、がんの進行へと繋がるケースがある。
- ●特徴として、腫瘍によっては「ほとんどの患者様で高発現」
PSMD10W 抑制RNA
- ●「PSMD10 (ガンキリン)抑制RNA」とは異なる受容体の2種をターゲットとしたもの
CDC6 抑制RNA
- ●通常、多くの細胞では無秩序な細胞分裂が行われないように細胞周期の途中で制御がかかる。
- ●がん細胞などにおいてはCDC6という酵素がこの制御を不能にし、細胞が無秩序に増殖する原因になるとされる。
PIK3CA 抑制RNA
- ●PIK3CA遺伝子変異は、特に乳がんで認められることがある体細胞変異です。
KRAS 抑制RNA
- ●RAS(ラス)は、細胞の増殖などに関わるタンパク質のひとつ。
- ●KRAS遺伝子の変異は膵がんの患者さんの95%以上、大腸がん、肺がん、多発性骨髄腫、子宮体がんでも確認されている。
BRAF 抑制RNA
- ●BRAF遺伝子変異は、細胞増殖の指令の伝達に関わるBRAF遺伝子の異常です。
MDM2 抑制RNA
- ●がん抑制因子であるp53の活動を抑制的に調節するタンパク質。
- ●MDM2が減る→p53が抑制されない。
CDK4 抑制RNA
- ●がん細胞などにおいてはCDKという酵素が活性化することで、細胞分裂の制御ができなくなっている。
- ●細胞分裂の制御を不能にしているサイクリン依存性キナーゼ(CDK)を阻害することで抗腫瘍効果をあらわす。
ステージ4におけるがん遺伝子治療の実績
これまで標準治療のみでは適応ができなかった末期がん患者様においても、遺伝子治療と組み合わせて行うことで、これらの治療の効果を高めたり、抗がん剤の投与量や放射線の照射量を減らし、副作用を軽減させる可能性もございます。
末期がんの患者様において遺伝子治療が特に有効な治療と考えられるポイントは、遺伝子治療を事前に行うことで抗がん剤治療や放射線治療の治療効果を増幅する効果が期待できる点です。 抗がん剤治療にしても放射線治療にしても、がん細胞に対して重篤な障害を人為的に与えることで細胞に問題を発生させ、その危険信号に気づいたがん抑制遺伝子を強制的に働かせてがん細胞をアポトーシスに導こうとする治療です。抗がん剤治療や放射線の効果が人により著しく異なるのは、細胞に問題を発生させてもそれに気づくべきがん抑制遺伝子がそのがん患者さんのがん細胞の中に正しく備わっていない場合があるからです。がん発生の原因は、がん抑制遺伝子の損傷にあることから抗がん剤治療や放射線治療を行っても、その仕組みが機能しにくいのもがん細胞の特徴と言えます。
遺伝子治療の特性や技術
ノーベル生理学・物理学賞を受賞した技術「RNA干渉」
がん抑制遺伝子の
損傷とがん発生のメカニズム
「がん」には、増えるとよくない物質(タンパク質)があります。
その「がん」の増殖を促進させるタンパク質を作るために、メッセンジャーRNA(mRNA)が増加します。このmRNAを抑制するRNAを投与することで、「がん」の増殖を促進させるタンパク質の発現を抑えて、細胞分裂の暴走を止めるようにコントロールする技術を「RNA干渉」といいます。
当クリニックでは、この技術を用いた治療も加えて行っています。
がん細胞にのみ集積する特性
「EPR効果」
EPR効果とはがん細胞にだけ薬剤を運ぶDDS(ドラッグデリバリーシステム)。
正常細胞の血管壁は通らず、がん細胞の血管壁のみ通るように、大きさを調整し、がん細胞にだけ薬剤を運びます。
新生血管は血管壁が正常血管よりも荒く、100~200nm(ナノメートル)程度の隙間が空いています。遺伝子治療に用いる治療タンパクや光免疫治療の光感作物質の大きさは、通常で1nm(ナノメートル)以下の低分子です。この大きさのまま体内に投与すると、正常血管からも漏れ出してしまい、がんになっていない正常な組織にも届いて細胞を破壊してしまいます。抗がん剤などで副作用が出るのはこのためです。
そこで、正常血管からは漏れ出さずに、新生血管からのみ漏れ出すように、薬剤等の大きさを
100nm(ナノメートル)程度に加工します。大きくなった薬剤等は、正常血管からは飛び出さず、新生血管からのみ飛び出すため、がん細胞に集中的に蓄積されます。さらに、漏れ出した薬剤等はふたたび血管内に戻りにくく、がん細胞周辺に留まります。