■未承認医薬品等であることの明示
本治療に用いる未承認医薬品等は、医薬品医療機器等法上の
承認を得ていないものです。
〒810-0041 福岡市中央区大名2-6-39 7F フリーダイヤル:0120-760-077 /TEL:092-707-1710
診療カレンダー・予約フォーム 診療カレンダー

分子標的(HER2)ワクチンとは体内で分子標的薬を作り出す最新の技術であり、海外で効果が立証されている新たな治療方法です。
保険診療の分子標的薬は効果が高くがん細胞を狙い撃ちできることが特徴ですが、その反面副作用が大きく、 また決まったがん種にしか使えませんでした。
一方、分子標的ワクチンは、体内で抗体を作り出すため副作用が少なく、
分子標的薬と同様の効果が期待できます。分子標的ワクチン療法は、ご自身の免疫の抗体を使ってがんを攻撃する治療方法です。
事前検査、筋肉注射を3回と効果測定の4回による通院ですので、患者様への精神的、身体的負担も少なく、さらに副作用も少ない治療です。
現在、標準治療を受けている患者様でも、受けることが可能な治療方法です。
HER2とはがん細胞の増殖に関与するタンパク質のことです。
HER2は正常細胞にも存在することもあり、細胞の増殖調整機能だと考えられていますが、過剰に発現し活性化することで、細胞増殖の制御が不可能になり正常細胞が、がん化します。
そのHER2の抗体を体内で作り、がん細胞を無くしていく治療がHER2ワクチン療法です。
この治療法では2種類のワクチンを同時に使用することで、ハーセプチン(トラスツズマブ)とパージェタ(ペルツズマブ)の結合部位に作用する抗体を産生させることで、W(ダブル)の効果が期待出来ます。
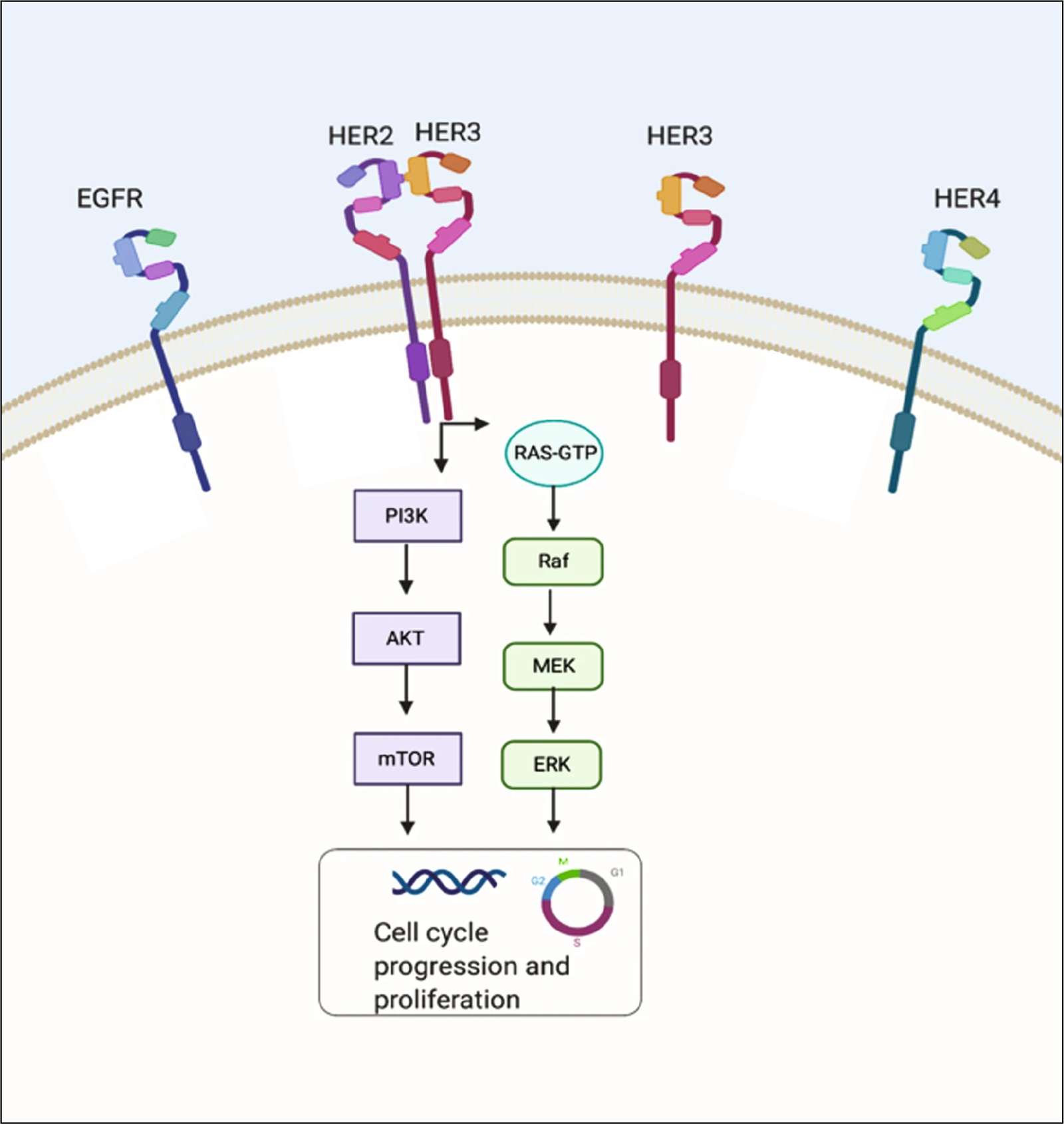
参考:Ilana Schlam & Sandra M. Swain. HER2-positive breast cancer and tyrosine kinase inhibitors: the time is now. npj Breast Cancer volume 7, Article number: 56 (2021)
狙い撃ち
がん細胞をピンポイントで攻撃します
(分子標的薬)
効果が持続
体の中の免疫が作用するので継続的な
効果が期待できます
体にやさしい
外部から取り入れた薬剤ではなく、自身の
免疫による治療のため体にやさしい
耐性がつきにくい
抗がん剤等よりも耐性がつきにくいため効果が
なくなって
しまうことが、抗がん剤等に比べて少ない。
メリット
デメリット
分子標的ワクチン療法のHER2ワクチン(3回/1クール)を受けた
がん患者様を対象とした治療実績【アメリカでの治験(Phase I)の結果】
以下の条件を満たす患者様についての結果。
対象のがん種:耳下腺がん、食道がん、肺がん、腹膜がん、 結腸がん、直腸がん、肛門がん、膀胱がん、乳がん、卵巣がん、子宮頸がん
■ワクチン 投与量
1回のワクチンにおいて、ハーセプチン結合部位ペプチドおよびパージェタ結合部位ペプチドをそれぞれ1mgまたは1.5mg投与した場合(16人)の結果
■結果
| 著効(がんが縮小) | 不変(がんの増大を30%以内) | 進行(30%以上増大) |
|---|---|---|
| 4人 | 11人 | 1人 |
| 治療有効率:93.75% | ||
※ワクチンの投与前、もしくは初めの投与から71日後に測定。
| 著効(がんが縮小) | 4人 | |
|---|---|---|
| 不変(がんの増大を30%以内) | 11人 | |
| 進行(30%以上増大) | 1人 | |
| 治療有効率:93.75% | ||
※ワクチンの投与前、もしくは初めの投与から71日後に測定。
■副反応
アメリカで PhaseI 臨床試験を受けた 49 人のがん(耳下腺がん、食道がん、肺がん、腹膜がん、 結腸がん、直腸がん、肛門がん、膀胱がん、乳がん、卵巣がん、子宮頸がん)患者様について以下 の副反応が報告されています。
| 副反応(患者数%) | グレード1-2 | グレード3-4 | 総数 |
|---|---|---|---|
| リンパ節の痛み | 1 (2%) | 0 (0%) | 1 (2%) |
| 疲れ | 4 (8%) | 0 (0%) | 4 (8%) |
| 発熱 | 2 (4%) | 0 (0%) | 2 (4%) |
| 感冒様症状 | 1 (2%) | 0 (0%) | 1 (2%) |
| 注射部位反応 | 12 (24%) | 0 (0%) | 12 (24%) |
| アレルギー反応(軽度の低血圧、発汗) | 1 (2%) | 0 (0%) | 1 (2%) |
| アラニントランスアミナーゼ上昇 | 1 (2%) | 0 (0%) | 1 (2%) |
| アルカリフォスファターゼ上昇 | 1 (2%) | 0 (0%) | 1 (2%) |
| リンパ球減少症 | 2 (4%) | 0 (0%) | 2 (4%) |
| 白血球減少症 | 1 (2%) | 0 (0%) | 1 (2%) |
| 低アルブミン血症 | 2 (4%) | 0 (0%) | 2 (4%) |
| 低ナトリウム血症 | 2 (4%) | 0 (0%) | 2 (4%) |
| 低リン血症 | 0 (0%) | 1 (2%) | 1 (2%) |
| 注射部位の痛み | 1 (2%) | 0 (0%) | 1 (2%) |
| 筋肉痛 | 2 (4%) | 0 (0%) | 2 (4%) |
| 皮膚乾燥 | 1 (2%) | 0 (0%) | 1 (2%) |
| 皮膚の痛み | 1 (2%) | 0 (0%) | 1 (2%) |
| かゆみ | 1 (2%) | 0 (0%) | 1 (2%) |
| 斑状丘疹状皮疹 | 1 (2%) | 0 (0%) | 1 (2%) |
| 皮膚および皮下組織障害 | 3 (6%) | 0 (0%) | 3 (6%) |
| 皮膚潰瘍 | 1 (2%) | 0 (0%) | 1 (2%) |
1.Kaumaya PT. B-cell epitope peptide cancer vaccines: a new paradigm for combination immunotherapies
with novel checkpoint peptide vaccine. Future Oncol. 2020; 16: 1767-1791. doi:
10.2217/fon-2020-0224.
2.Bekaii-Saab T. et al. Phase I immunotherapy trial with two chimeric HER-2 B-cell peptide vaccines
emulsified in Montanide ISA 720VG and nor-MDP adjuvant in patients with advanced solid tumors. Clin.
Cancer Res. 2019; 25: 3495-3507. doi: 10.1158/1078-0432.CCR-18-3997.
3.Graus-Porta D. et al. ErbB-2, the preferred heterodimerization partner of all ErbB receptors, is a
mediator of lateral signaling. EMBO J. 1997; 16: 1647-1655. doi: 10.1093/emboj/16.7.1647.
4.Kinugasa H. et al. Droplet digital PCR measurement of HER2 in patients with gastric cancer. Br. J.
Cancer. 2015; 112: 1652-1655. doi: 10.1038/bjc.2015.129
01.
インフォームド・コンセント(治療説明)
医師から治療内容について患者様に十分理解していただける様に説明します。
02.
スケジュールの決定、料金、同意書について
コーディネーターと患者様で相談し、スケジュールを決めます。その際に料金や同意書についてご説明いたします。
03.
お支払い
事前のお支払いをお願いしております。お振込み、クレジットカードもご利用できます。
04.
治療
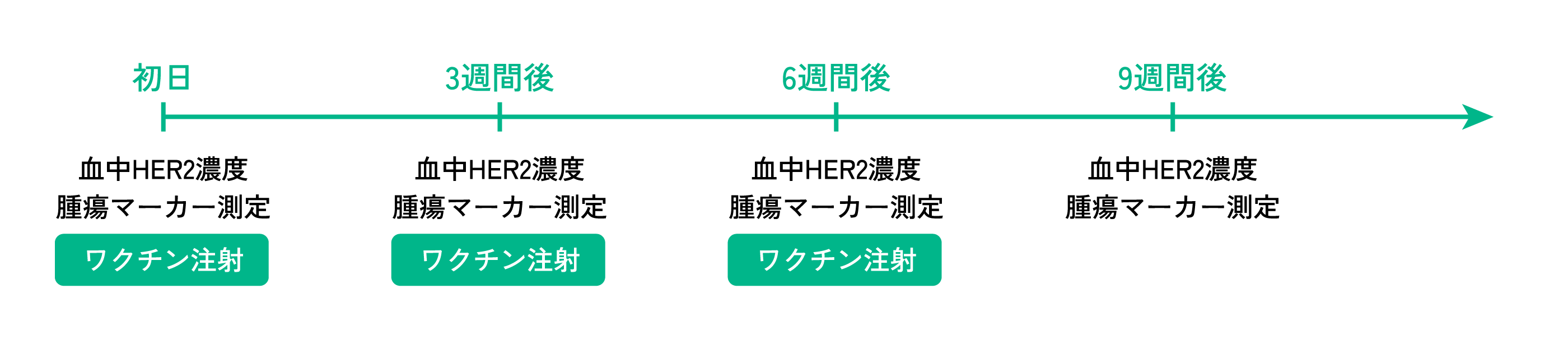
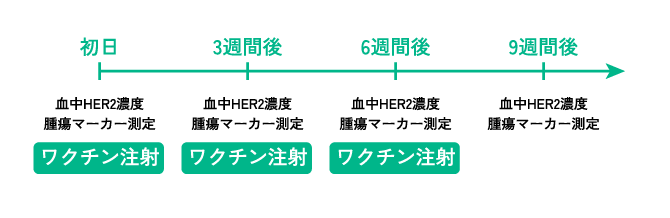
通院での治療です。筋肉注射を3週間に1回ずつ3回行い、3回目の3週間後に血液検査で効果測定を行います。
05.
治療効果の評価
血液検査で治療効果を評価し、今後の治療をご提案いたします。
| 治療項目 | 治療回数 | 合 計 |
|---|---|---|
| 1クール目 | 3回 | 1,980,000円(税込み) |
| 治療項目 | 1クール目 |
|---|---|
| 治療回数 | 3回 |
| 合 計 | 1,980,000円(税込み) |


発熱、アレルギー
ごく稀に点滴物質への免疫反応として悪寒発熱等の副作用が発生する可能性がございます。また、アレルギー体質の方の中に一部アレルギー反応が生じる場合がございます。
アナフィラキシーショック等重篤な症状が出る可能性もございます。


妊婦
妊婦において安全性はまだ確立しておりません。妊娠中あるいは妊娠の可能性がある方は基本的にお断りさせて頂いております。
全てのがんの根治に繋がるものではありません。他の治療と同様に、全てのがんに対し、根治をお約束することはできかねます。
しかしながら、患者様の状況を判断し最善をご提案いたします。
■未承認医薬品等であることの明示
本治療に用いる未承認医薬品等は、医薬品医療機器等法上の
承認を得ていないものです。
■入手経路の明示
国内研究所経由で入手し、最終調合を院内で行っています。
■国内の承認医薬品等の有無の明示
本治療に使用できる同一の性能を有する他の国内承認医薬品はありません。